Índice de contenidos
El papel de las interrupciones AGG en la expansión de tripletes asociada a X frágil
La capacidad de predecir la probabilidad de expansión de los tripletes CGG en el gen FMR1 generando una mutación completa (>200 CGGs) es de vital importancia para el consejo genético de mujeres portadoras de alelos premutados (55-200 CGGs), ya que su descendencia tiene el riesgo de sufrir el síndrome X frágil.
Se ha demostrado que estos elementos AGG confieren estabilidad a la secuencia del gen y por tanto reducen el riesgo de expansión de las repeticiones CGG durante la transmisión materna.
El gen FMR1
El gen FMR1 (Fragile X Mental Retardation 1) se localiza en el cromosoma X y codifica la proteína FMRP, que es esencial para el desarrollo cerebral y la plasticidad sináptica. En la región 5’ no codificante del gen se encuentra una zona de tripletes CGG, cuya expansión por encima del rango normal (5-44 CGGs) da lugar a un amplio espectro de trastornos asociados al cromosoma X frágil.
El colegio americano de genética médica (ACMG) clasifica los posibles alelos de este gen en 4 categorías: Normal (<45 CGGs), Intermedia (45-54 CGGs), Premutación (55-200 CGGs) y Mutación completa (>200 CGGs). Con mayor frecuencia los alelos con mutación completa, aunque también algunos premutados, están metilados en la zona de las repeticiones. Como consecuencia se produce la inactivación del gen, la ausencia de la proteína FMRP y el desarrollo del síndrome de X frágil.
Por otro lado, parece que la clínica de los trastornos asociados a los alelos premutados, como son el síndrome de temblor/ataxia y el síndrome de insuficiencia ovárica primaria, es debida a la sobre-expresión del mRNA de FMR1. Esto da lugar a una toxicidad por este RNA y a menudo a reducciones de FMRP.
Inestabilidad de las regiones CGG
Aunque la repetición CGG es muy estable cuando se transmite desde individuos con alelos normales, es significativamente inestable en la transmisión materna de los alelos premutados (55-200 CGGs), que con frecuencia se expanden a una mutación completa en la siguiente generación.
Desde la identificación del gen en 1991, la estimación del riesgo de expansión se ha basado en el número de repeticiones del alelo materno. Más del 94% de los alelos con más de 90 CGGs se expanden a mutación completa. Por esta razón, muchas mujeres embarazadas se someten a screening de portadoras independientemente de la historia familiar.
Además, hay que tener en cuenta la elevada frecuencia de los alelos premutados entre las mujeres en la población general, que es de 1/150-250.
La inestabilidad de la zona de repeticiones durante la transmisión parental favorece la expansión del fragmento CGG.
Aunque la base de la inestabilidad es desconocida, se piensa que elementos cis y trans pueden jugar algún papel en la expansión de tripletes. Algunos factores trans incluyen enzimas reparadoras de DNA, estudiadas en modelos animales de la enfermedad de Hungtington y de X frágil.
El mecanismo propuesto se basa en errores de estas enzimas cuando se produce un daño oxidativo del DNA, aunque no se conoce exactamente cómo esto contribuye a la expansión de los tripletes.
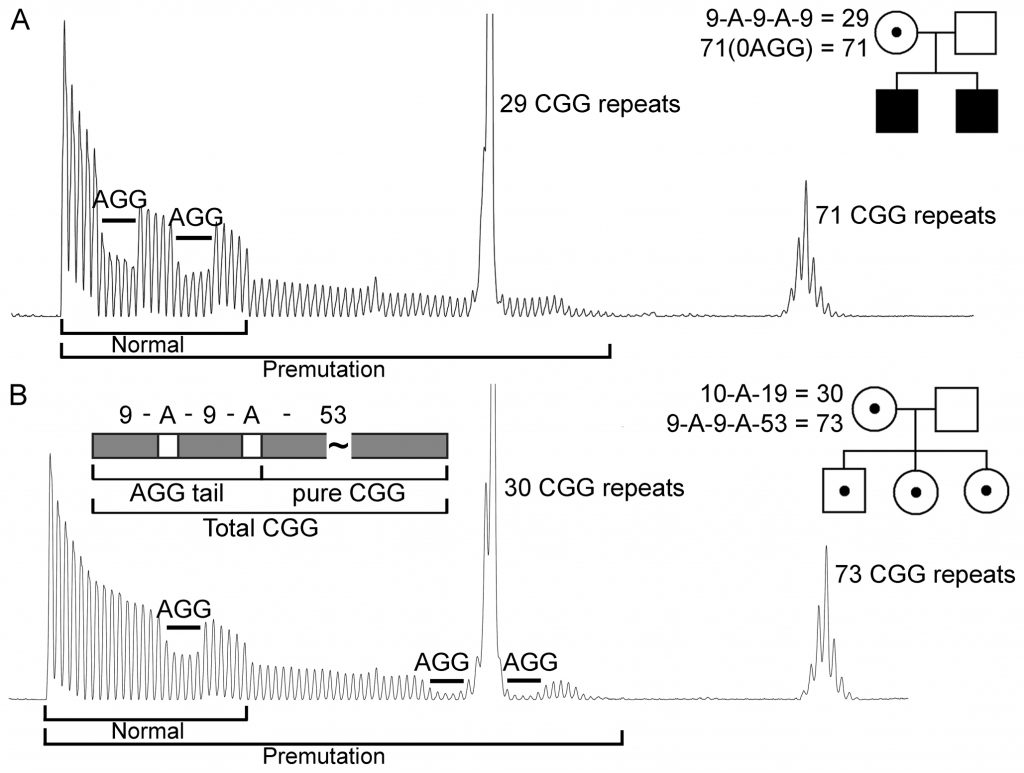
En 1994, Eichler y colaboradores sugirieron que los elementos cis AGG intercalados en la región CGG del gen FMR1 aumentaban la estabilidad de esta zona. Sin embargo, hasta hace poco la presencia de las AGGs no se ha podido estudiar a gran escala debido a la falta de una técnica precisa para detectarlas. En estos momentos se dispone de la técnica TP-PCR (Chen y cols., 2010) para identificar el número y la posición de estas AGGs.
Cómo influyen las interrupciones AGG en la expansión de tripletes
En la población general, el 94% de los alelos tienen una o dos interrupciones AGG, las cuales están típicamente separadas por 9-11 CGGs y se observan en el extremo 5’ de la región de repeticiones CGG. Así, los alelos normales suelen tener 2 o 3 AGGs y los premutados entre 0 y 2 AGGs. Los individuos con historia familiar de X frágil suelen carecer de estas interrupciones.
Estudios biofísicos han revelado distintas estructuras para las secuencias de CGG sin interrupciones, comparadas con aquellas conteniendo elementos AGG. Por ejemplo, oligonucleótidos de hasta 39 repeticiones CGG forman estructuras en “horquilla” muy estables. Los elementos AGGs alterarían estas configuraciones que no tienen estructura de DNA-B y actuarían como un freno para detener la expansión de (Jarem y cols., 2010).
Gracias a la amplificación de la región CGG del gen FMR1 mediante TP-PCR se han realizado muchos estudios, sobre todo en mujeres premutadas, para determinar el riesgo de expansión a mutación completa. Todos ellos concluyen que la presencia de AGGs aumentan significativamente la estabilidad genética y que los alelos sin AGGs tienen el riesgo más alto de expansión (Nolin y cols., 2011; Nolin y cols., 2014; Yrigollen y cols., 2012).
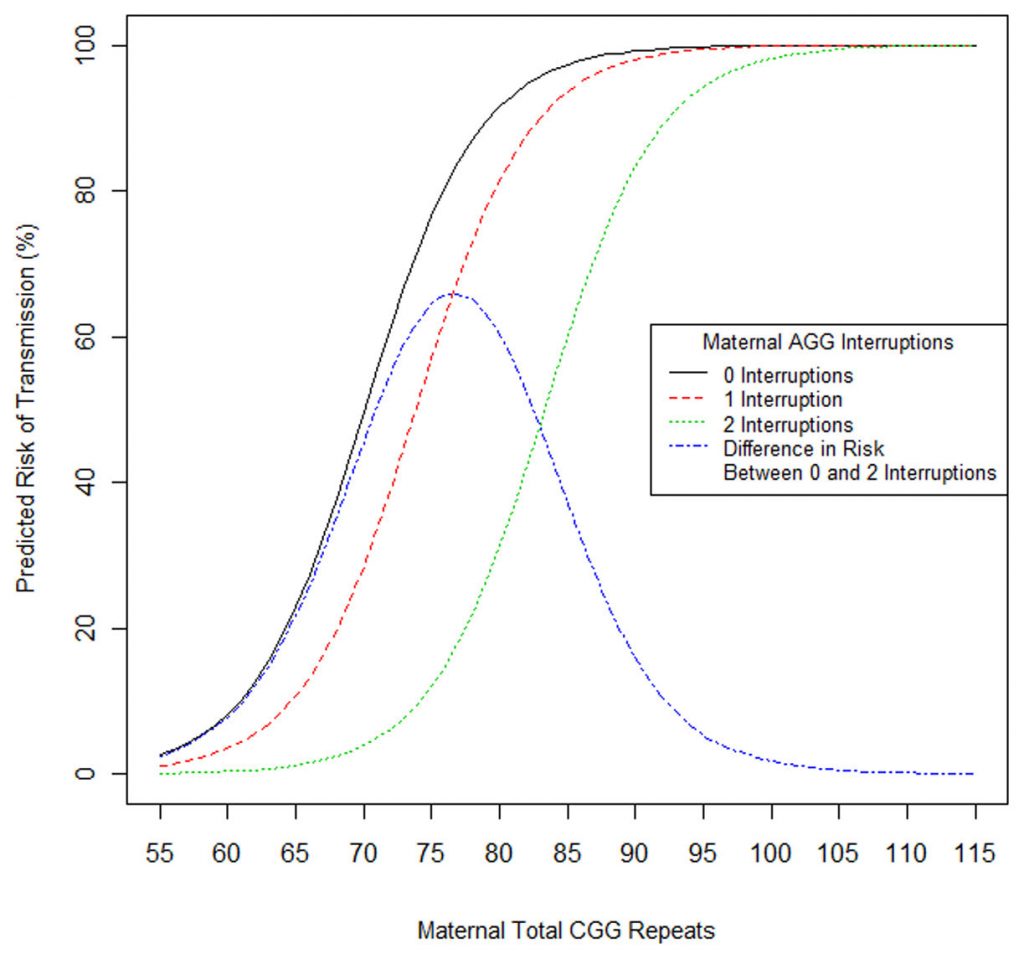
Se demostró que la presencia de AGGs reducía el riesgo de expansión a mutación completa para todos los alelos premutados maternos por debajo de 100 repeticiones, con una diferencia de más del 60% (0 vs 2 AGGs) en el rango de 70-80 CGGs. Por ejemplo, para un alelo de 75 CGGs sin ninguna AGG el riesgo de expansión se estima en 77%, sin embargo se reduce a 12% si contiene 2 AGGs.
Información de las AGGs en el consejo genético
La estimación del riesgo de expansión para alelos entre 45-90 repeticiones CGG ha sido un punto crítico en el consejo genético. La influencia demostrada de las AGGs en la estabilidad genética y la técnica TP-PCR para detectar estas interrupciones permiten ahora mejorar dicha estimación.
Por ello en las guías de práctica clínica se recomienda la determinación del número de CGGs y el número/posición de AGGs para la evaluación del riesgo de expansión del síndrome X frágil.
Además, la detección de las AGGs será de gran utilidad en los alelos intermedios de 45 a 54 CGGs (denominados también en “zona gris”) y en premutados con bajo número de CGGs, cuya estabilidad es aún más incierta.
En cualquier caso, en el consejo genético siempre se deberá informar que se trata de una estimación y que la presencia de AGGs no elimina el riesgo de expansión, ya que puede haber otros factores (cis o trans) que contribuyan a modificar el riesgo de sufrir el síndrome X frágil.
Artículos relacionados
Efectos de un bajo número de repeticiones CGG en el gen FMR1