La secuenciación WES o secuenciación del exoma completo, permite secuenciar el exoma con la finalidad de detectar de forma simultánea mutaciones o variaciones en individuos con trastorno del espectro autista (TEA).
Índice de contenidos
Trastornos del espectro autista (TEA)
Los trastornos del espectro autista (TEA) aparecen en la infancia y se caracterizan por un déficit en la comunicación social acompañados de comportamientos o intereses restringidos y repetitivos. Afectan a más del 1% de individuos1.
Muchos estudios hasta la fecha han demostrado su alta heredabilidad, mayormente debido a variaciones comunes2, aunque son las variantes raras y de novo las que más contribuyen al riesgo individual. Cuando una variación rara aparece siempre en un mismo gen en individuos con TEA, implica que este es un gen de riesgo3.
Estudios del trastorno del espectro autista
En el estudio del trastorno del espectro autista más amplio hasta la fecha4 se ha secuenciado el exoma completo (WES) de 35.584 personas, 11.986 con TEA. En este informe, se han identificado 9.345 variantes raras de novo y se ha demostrado que el tipo de variante genética también tiene un peso considerable en su relación con el TEA. Son, por ejemplo, variantes proteicas truncadas (PTVs) como nonsense, frameshift y variantes de splicing muestran una mayor diferencia entre el grupo con TEA y el grupo control que, por ejemplo, las mutaciones missense.
En dicho estudio se identificaron 102 genes de riesgo. De esos genes, 49 muestran altas frecuencias de variantes de novo disruptivas en individuos con discapacidad intelectual severa mientras que 53 muestran alta frecuencias en individuos con TEA. La mayoría de estos genes tienen un papel importante en la regulación de la expresión génica y/o en la comunicación neuronal.
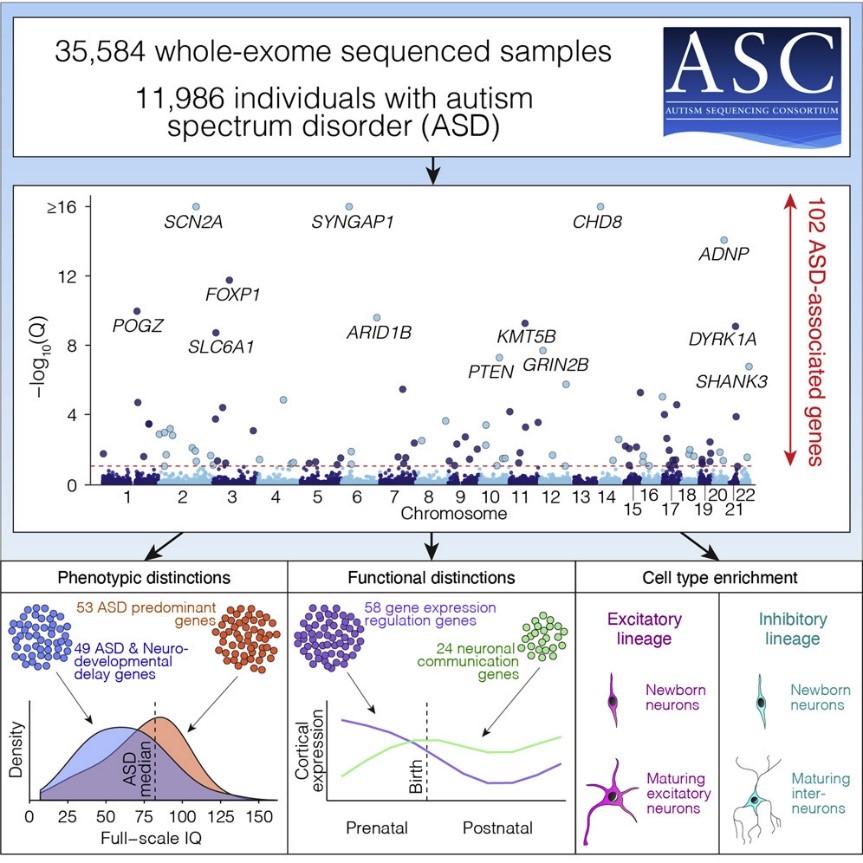
Entre las mutaciones observadas, el radio de PTVs con respecto a mutaciones missense varía sustancialmente entre genes. Algunos genes como ADNP alcanzan el umbral de asociación solamente con PTVs, mientras que otros tres genes, SYNGAP1, DYRK1A y ARID1B, tienen un exceso significativo de PTVs con respecto a mutaciones missense. Por el contrario, también se asociaron genes al TEA basándose únicamente en variaciones missense de novo. En concreto, 4 genes con 4 o más variantes missense de novo y solamente una o ninguna PTVs: DEAF1, KCNQ3, SCN1A y SLC6A1.
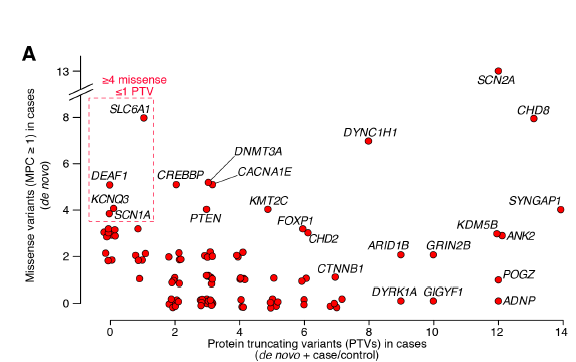
Imagen 2. PTVs versus variantes missense para cada gen asociado a TEA.
La prevalencia del TEA es cuatro veces mayor en hombres que en mujeres. Se ha comentado que las mujeres poseen un efecto protector ya que las mujeres requieren una carga genética mayor de PTVs para alcanzar el umbral del diagnóstico5. Las variaciones en el número de copias (CNV) representa un riesgo importante de TEA6, pero estos desordenes genéticos pueden incluir docenas de genes, complicando así la identificación de los genes principales en esas regiones.
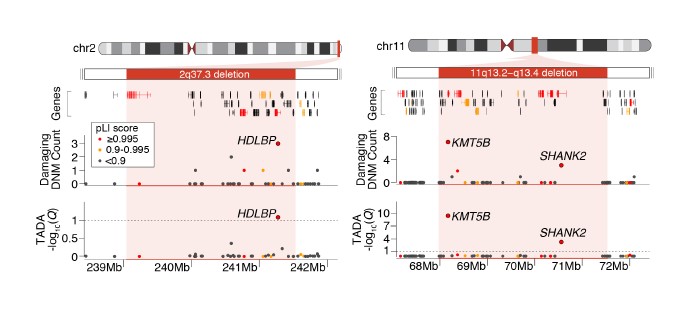
Variaciones comunes en Trastorno del espectro autista
Las variaciones comunes juegan un papel importante en el riesgo de TEA. Un estudio reciente de asociación del genoma completo (GWAS) ha revelado una serie de loci asociados al TEA7. Los estudios familiares han estimado una alta heredabilidad en el TEA8, pero que comparada con la heredabilidad estimada en casos severos de trastornos del desarrollo neurológico es menor 8.
De acuerdo con esta información, los estudios de exoma han identificado una mayor frecuencia de variantes disruptivas de novo en casos severos de discapacidad intelectual que en TEA. Existe una alta comorbilidad entre el TEA y la discapacidad intelectual y no es ninguna sorpresa que existan muchos genes asociados a ambas disfunciones. Distinguir genes que se dirigen más frecuentemente a TEA que a discapacidad intelectual puede dar más luz dentro de lo atípico de este desorden neurológico.
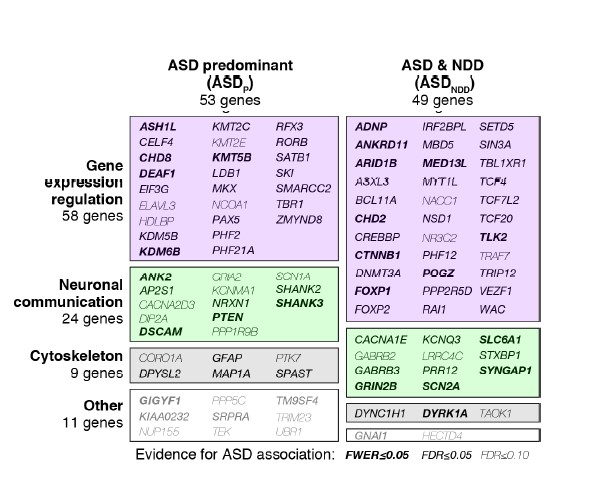
IEn el estudio de secuenciación de exoma comparando individuos con TEA e individuos control más amplio hasta la fecha4 se han dividido los genes objeto de estudio en genes predominantemente asociados al TEA y genes asociados al TEA con discapacidad intelectual.
Esta distinción es muy importante para médicos, genetistas y neurólogos porque saber el impacto que provocan estos genes puede permitir discernir entre el TEA y otros trastornos neurológicos. Son necesarios estudios de secuenciación de exomas más amplios para identificar con más confianza genes específicos.
Referencias
- Baio, J., et al. (2018). Prevalence of Autism Spectrum Disorder Among Children Aged 8 Years – Autism and Developmental Disabilities Monitoring Network, 11 Sites, United States, 2014. MMWR Surveill Summ 67, 1-23.
- Gaugler, T., et al. (2014). Most genetic risk for autism resides with common variation. Nature genetics 46, 881-885.
- He, X., et al. (2013). Integrated model of de novo and inherited genetic variants yields greater power to identify risk genes. PLoS genetics 9, e1003671.
- F. Kyle Satterstrom, et al. (2020). Large-Scale Exome Sequencing Study Implicates Both Developmental and Functional Changes in the Neurobiology of Autism
- Werling, D.M. (2016). The role of sex-differential biology in risk for autism spectrum disorder. Biology of Sex Differences 7, 1-18.
- Sebat, J., et al. (2007). Strong association of de novo copy number mutations with autism. Science (New York, NY) 316, 445-449.
- Grove, J., et al. (2019). Identification of common genetic risk variants for autism spectrum disorder. Nature genetics.
- Yip, B.H.K., et al. (2018). Heritable variation, with little or no maternal effect, accounts for recurrence risk to autism spectrum disorder in Sweden. Biological psychiatry 83, 589-597.
- Reichenberg, A., et al. (2016). Discontinuity in the genetic and environmental causes of the intellectual disability spectrum. Proceedings of the National Academy of Sciences 113, 1098-1103.
Artículos relacionados
NGS como herramienta en la biopsia líquida
Trastornos del neurodesarrollo a partir de la Secuenciación del Genoma como técnica de primer nivel
Tecnología NGS como herramienta de control en infecciones nosocomiales
Farmacogenética, hacia una terapia personalizada
Secuenciación de genomas: Historia y estado actual
El uso de las técnicas rápidas de diagnóstico por secuenciación masiva ya está aquí

